
Hoá học 11 Bài 40: Ancol
1.1.1. Định nghĩa
- Ancol là hợp chất hữu cơ mà trong phân tử có nhóm hiđroxyl (-OH) liên kết trực tiếp với nguyên tử cacbon no của gốc hiđrocacbon.
- Ví dụ: CH3OH, C2H5OH, CH3CH2CH2OH, CH2=CHCH2OH, C6H5CH2OH ...
1.1.2. Phân loại
a) Phân loại Ancol
Cơ sở phân loại Phân loại Ví dụ Theo gốc hidrocacbon Ancol no CH3OH, C2H5OH Ancol không no CH2=CH-CH2-OHAncol thơm
C6H5OH, C6H5CH2OHTheo số nhóm -OH
Ancol đơn chức CH3OH, CH2=CH-CH2-OH Ancol đa chức (CH2)2(OH)2 Theo bậc ancolAncol bậc I
CH3-CH2-OH Ancol bậc II Ancol bậc IIIb) Một số loại ancol tiêu biểu
- Ancol no mạch hở, đơn chức: có nhóm -OH liên kết trực tiếp với gốc ankyl
VD: CH3OH, C2H5OH,...,CnH2n - OH
- Ancol không no, mạch hở, đơn chức: có nhóm -OH liên kết với nguyên tử cacbon của gốc hiđrocacbon không no
VD: CH2 = CH - CH2 - OH
- Ancol thơm đơn chức: có nhóm -OH liên kết với nguyên tử cacbon no thuộc mạch nhánh của vòng Benzen
VD: C6H5 - CH2 - OH: ancolbenzylic
- Ancol vòng no, đơn chức: có nhóm -OH liên kết với nguyên tử cacbon no thuộc hiđrocacbon vòng no
VD: xiclohexanol
- Ancol đa chức: phân tử có hai hay nhiều nhóm -OH
VD: (Etilen glicol); (glixerol)
1.2.1. Đồng phân
- Có 2 loại:
- Đồng phân về vị trí nhóm chức
- Đồng phân về mạch cacbon
- VD: Viết các đồng phân ancol có công thức: C4H9OH
1.2.2. Danh pháp
a) Tên thông thường (gốc - chức)
- Ví dụ:
CH3 - OH (Ancol metylic)
CH3 - CH2 - OH (ancol etilic)
CH3 - CH2 - CH2 - OH (ancol propylic)
- Nguyên tắc: Ancol + tên gốc ankyl + ic
b) Tên thay thế
- Ví dụ:
CH3-OH: metanol
CH3-CH2-OH: Etanol
CH3-CH2-CH2-CH2-OH: butan-1-ol
: 2-metylpropan-1-ol
- Chú ý:
- Mạch chính được quy định là mạch cacbon dài nhất chứa nhóm OH.
- Số chỉ vị trí được bắt đầu từ phía gần nhóm -OH hơn.
- Nguyên tắc: Tên hidrocacbon tương ứng mạch chính + số chỉ vị trí nhóm OH (nếu có) + "ol"
- Ancol là chất lỏng hoặc rắn, tan được trong nước
- Độ tan tỉ lệ nghịch với phân tử khối
- Nhiệt độ sôi tỉ lệ thuận với phân tử khối.
- Liên kết hiđro: Nguyên tử H mang một phần điện tích dương ({delta ^ + }) của nhóm -OH này khi ở gần nguyên tử O mang một phần điện tích ({delta ^ - }) của nhóm -OH kia thì tạo thành một liên kết yếu gọi là liên kết hiđro, biểu diễn bằng dấu...
Hình 1: Liên kết Hidro
a) Giữa các phân tử ancol với nhau
b) Giữa các phân tử ancol với các phân tử nước
- Ảnh hưởng của liên kết hiđro đến tính chất vật lí: liên kết hidro làm cho ancol có nhiệt độ sôi cao hơn, tan nhiều trong nước hơn.
Trong phân tử, liên kết C OH đặc biệt liên kết O H phân cực mạnh nên nhóm -OH, nhất là nguyên tử H dễ bị thay thế hoặc tách ra trong phản ứng hóa học.
Hình 2: Mô hình phân tử etanol
a) Dạng đặc b) Dạng rỗng
1.4.1. Phản ứng thế H của nhóm -OH
a. Tính chất chung của ancol
- Tác dụng với kim loại kiềm:
- Phương trình tổng quát: R-OH+ Na(K)→R-ONa + 1/2H2
Video 1: Phản ứng của etanol với Natri
Natri phản ứng với etanol tạo khí hidro: 2C2H5-OH +2Na →2C2H5-ONa + H2
Đốt khí thoát ra ở đầu vuốt nhọn, hidro cháy với ngọn lửa xanh mờ: 2H2 + O2 H2O
b. Tính chất đặc trưng của glixerol
- Phản ứng này cần sử dụng Cu(OH)2 mới sinh, do đó khi cần tiến hành thí nghiệm người ta mới điều chế Cu(OH)2
- Phương trình phản ứng:
CuSO4 + 2NaOH → Cu(OH)2 + Na2SO4
Hòa tan Cu(OH)2 tạo dd màu xanh lam.
2C3H5(OH)3 + Cu(OH)2 → [C3H5(OH)2O]2Cu +2H2O.
Đồng (II)glixerat
Hình 3: Glixerol hòa tan Đồng (II) hidroxit thành dung dịch màu xanh lam (2)
Etanol không có tính chất này (1)
Video 2: Glixerol tác dụng với Cu(OH)2
⇒ Phản ứng này được dùng để phân biệt ancol đơn chức với ancol đa chức có các nhóm -OH cạnh nhau trong phân tử.
1.4.2. Phản ứng thế nhóm -OH
a. Phản ứng với axit vô cơ
C2H5-OH + HBr C2H5-Br + H2O
b. Phản ứng với ancol
C2H5-OH + H-OC2H5 C2H5-O-C2H5 + H2O
đietyl ete (ete etylic)
1.4.3. Phản ứng tách nước
CH3-CH2-OH CH2=CH2 + H2O
⇒ Tính chất này được ứng dụng để điều chế anken từ các ankanol
1.4.4. Phản ứng oxi hóa
a. Oxi hóa không hoàn toàn
- Ancol bậc 1→ andehit (-CH→O)
VD: C2H5OH + CuO CH3-CHO + H2O.
- Ancol bậc 2: → xetôn (>C→O)
VD: CH3-CH(OH)-CH3 + CuO CH3-CO-CH3 + H2O
- Trong điều kiện như trên các ancol bậc 3 không bị oxi hóa.
b. Oxi hóa hoàn toàn
- Cháy tỏa nhiều nhiệt
- Phương trình tổng quát: CnH2n+1-OH + 3n/2O2 nCO2 + (n+1)H2O
1.5.1. Phương pháp tổng hợp
- Etanol tổng hợp từ etylen: C2H4 + H2O C2H5-OH
- Tổng hợp ancol bằng cách thủy phân dẫn xuất halogen:
C2H5-Br + NaOH 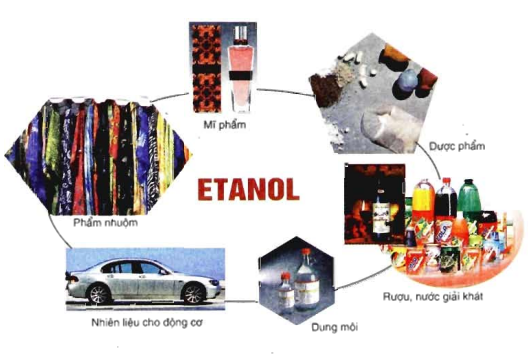
- Glixerol tổng hợp từ propilen
1.5.2. Phương pháp sinh hóa
(C6H10O5)n + nH2O nC6H12O6
C6H12O6 2C2H5OH + 2CO2
Hình 4: Ứng dụng của Ancol
Link nội dung: https://trungtamgiasuhanoi.edu.vn/bai-40-ancol-a31515.html